На исторической ленте самый большой временной интервал занимает термин «гастрит», но за последние десятилетия для объяснения тех или иных симптомов, изменений клеток слизистой желудка были выработаны понятия «гастропатия» и «функциональная диспепсия», помогающие глубже понять природу заболеваний желудка. Тому поспособствовали технологический прорыв, упорные поиски истины учеными, а возможно где-то и фортуна.
Первое упоминание о гастрите - в работах немецкого врача Шталя в «Collegium practicum» в 1732 году, который отметил, что некоторые лихорадочные заболевания связаны с поверхностным раздражением желудка и склонностью к язвам. DOI:10.3748/wjg.v30.i13.1851
Но история термина «хронический гастрит» берёт начало в работах французского врача Бруссе, в своей книге «История хронических флегмон или воспалений» (1808) он описал распространённые воспаления желудка, которые обнаруживались почти у каждого умершего солдата. Он назвал их «гастритами», и выделил гастрит в отдельную нозологическую форму.
Диагностика гастрита на живом человеке стала возможной после изобретения Шиндлером (всего лишь однофамилец того самого) гастроскопа в 1932 году. В своей монографии «Гастрит» он классифицировал гастрит на известные: на острый и хронический, а хронический на поверхностный, атрофический и гипертрофический.
Значимой вехой в изучении гастритов стало событие, когда Pelayo Correa и M Blanca Piazuelo в 1975г представили знаменитый каскад Корреа, в котором постулируется "переход" слизистой желудка поэтапно от воспаления, через атрофию и метаплазию к дисплазии и неоплазии (аденокарциноме).
Считается, что первыми, кто обнаружил колонии спиралевидных бактерий (хеликобатер) на дне язв в желудке собак, были немецкий бактериолог Боттхер и его коллега Лютюлле в 1875 году.
В 1994 году Международное агентство по исследованию рака (IARC) классифицировало Helicobacter pylori в качестве канцерогена 1-й группы.
Учитывая опыт, накопленный во всем мире за более чем 15 лет ( с 1990 –го года) применения Сиднейской системы, международная группа патологоанатомов (Operative Link for Gastritis Assessment) предложила систему классификации гастрита по стадиям (система OLGA). Стадии гастрита классифицируют гистологические фенотипы гастрита по шкале прогрессивно возрастающего риска развития рака желудка, от самого низкого (стадия 0) до самого высокого (стадия IV). PMID: 18424244 DOI: 10.1016/j.dld.2008.02.030
Gо данной системе исследованию подвергаются 5 биоптатов: два образца биопсии выполняются из антральной части желудка на расстоянии 2–3 см от привратника по малой и большой кривизне, один образец биопсии - из угла желудка и два образца биопсии - из тела желудка на расстоянии 8 см от розетки кардии по малой и большой кривизне. PMID: 19067779 DOI: 10.1111/j.1440-1746.2008.05679.x
Существует также аналогичная система OLGIM (Operative Link for Gastritis Intestinal metaplasia Assessment) для оценки распространения кишечной метаплазии. Целями данных систем были: преобразование гистопатологических данных в стандартизированный отчёт, отражение информации о состоянии желудка (топографии и степени атрофических изменений), а также стратифицировать пациентов по группам риска развития рака желудка.
В европейском исследовании долгосрочного наблюдения ни у одного пациента с OLGA/OLGIM 0–II стадии не развился рак желудка в течение 51 месяца наблюдения. Таким образом, эндоскопическое наблюдение каждые три года для пациентов со стадией III–IV, оцененной по OLGA/OLGIM, представляется достаточным в регионах с низким и средним уровнем заболеваемости раком желудка. DOI 10.33978/2307-3586-2024-20-2-54-70
Из вышеизложенных данных вытекает постулат о том, что гастрит-морфологический диагноз, который имеет определенную стадийность, этиологию (самая частая из которых, конечно же Helicobacter pylori), распространенность (она же топография), и риски появления новообразований.
Эндоскопические возможности и мощности со временем также нарастают. Эндоскопическая эпоха, начавшись примерно с 1949 года, когда Вуд и др. сообщили об изобретении простой биопсийной трубки, а затем в 1957 году, когда Хиршовиц изобрёл гибкий оптоволоконный фиброгастроскоп, который позволял проводить прицельную биопсию щипцами под визуальным контролем из любой части желудка, прошло немало времени, и на данный момент развития эндоскопический мир может предоставить пациентам эндоскопию высокого разрешения с улучшенными методами визуализации как: NBI, FICE , виртуальная хромоэндоскопия и др.
Современная оптика эндоскопов экспертного уровня позволяет определить: нормальная слизистая желудка перед нами, атрофичная, измененная по типу метаплазии или с диспластическими изменениями, но помним, что все в медицине оператор- и технически зависимое.
Нормальная эндоскопическая картина может быть трудноопределимой, и отсутствие поражений или изменений обычно считается адекватным синонимом. Однако существует признак, заключающийся в регулярном расположении собирательных венул в дистальном отделе желудка при использовании стандартной эндоскопии высокого разрешения – белым светом или интегрированной эндоскопии в виде регулярно распределенных красных точек или сосудистых структур типа «морской звезды». Наличие таких признаков имеет положительную прогностическую ценность более 90% в отношении наличия нормальной кислотопродуцирующей слизистой желудка и надежно исключает инфекцию H. pylori.
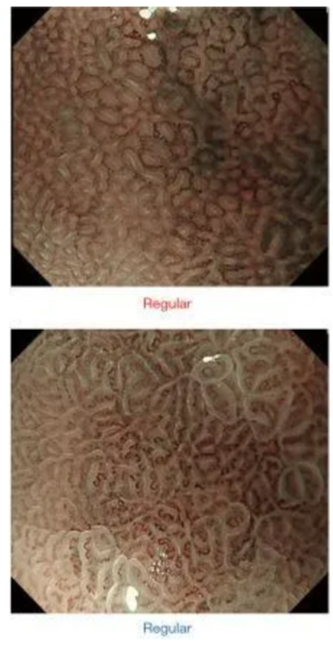
Рис 1. Из Muto M, Yao K, Kaise M, et al. Magnifying endoscopy simple diagnostic algorithm for early gastric cancer (MESDA-G). Dig Endosc 2016;28:379-93
Согласно данным, опубликованным в литературе, чувствительность и специфичность обычной эндоскопии с использованием белого света для диагностики атрофии слизистой оболочки желудка составляют 53–59%, а чувствительность и специфичность эндоскопии с использованием белого света высокой чёткости с увеличением — 70–74%. С точки зрения чувствительности и специфичности эндоскопия с улучшенным изображением превосходила обычную эндоскопию с использованием белого света. В частности, согласно результатам метаанализа, в исследованиях с использованием узкополосной визуализации (NBI), чувствительность диагностики кишечной метаплазии составила 0,78 (95% ДИ, 0,69–0,89), а специфичность — 0,89 (95% ДИ, 0,84–0,92) без использования увеличительной эндоскопии. Таким образом, ожидается, что методы эндоскопии с улучшенным изображением, такие как NBI, будут очень полезны при эндоскопической диагностике метаплазии кишечного эпителия. PMID: 24743566 PMCID: PMC3990530 DOI: 10.1371/journal.pone.0094869
Рекомендации MAPS II (Европейские рекомендации по ведению пациентов с предраковыми изменениями в желудке, 2019 г) с высоким уровнем доказательности (94%) и согласованности (94%) рекомендуют для диагностики предраковых и ранних неопластических изменений слизистой оболочки желудка проводить эндоскопию именно высокого разрешения с хромоэндоскопией, а не эндоскопию высокого разрешения с использованием белого света.
Отвечая на вопрос –а возможно ли поставить диагноз атрофии и/или кишечной метаплазии при помощи эндоскопических методов обследования? Да, атрофированная слизистая и кишечная метаплазия могут быть точно определены с помощью эндоскопии с улучшением изображения специалистами, имеющими соответствующий уровень подготовки. PMID: 38383142 DOI: 10.1136/gutjnl-2023-331164
Обычная эндоскопия в большинстве случаев не подходит для диагностики атрофии и кишечной метаплазии, и, следовательно, биопсия остается обязательной процедурой, позволяющей судить о гистоморфологической структуре слизистой желудка согласно Сиднейской классификации. Тем не менее эндоскопия с улучшением изображения повысила точность и воспроизводимость эндоскопической диагностики предраковых поражений желудка. К ней относится: хромоэндоскопия , эндоскопия в высоком разрешении c увеличением и эндоскопия с улучшенным изображением, комбинированная с увеличением. Адекватная оценка состояния слизистой желудка каждым из этих методов требует соответствующего обучения.
Хромоэндоскопия (ХЭ) — это метод внутрижелудочной эндоскопии, при котором на поверхность слизистой оболочки желудка распыляются красители для улучшения визуализации исследуемых образований.
Виртуальная или электронная хромоэндоскопия — это методы визуализации, позволяющие детально исследовать слизистую оболочку желудка. Их использование повышает эффективность диагностики предраковых изменений и позволяет эндоскописту выбирать «подозрительные» на кишечную метаплазию или дисплазию участки для взятия образцов гастробиопсии без использования красителей.
Гастропатия.
Данный термин был введен Зденеком Маржаткой в 1984г., и именно с помощью данного термина была создана минимальная стандартная терминология OMED. Для описания изменений слизистой желудка существует несколько типов гастропатий, на данный момент они отражены в классификации МСТ 3.0. (минимальная стандартная терминология).
В контексте диагностики гастрита, это: эритематозная, геморрагическая, эрозивная и гипертрофическая гастропатии, гастропатия, связанная с приемом нестероидных проивовоспалительных препаратов, гастропатия портальной гипертензии и оспоподобная гастропатия. (Аникина М.С. 2019г. https://endoexpert.ru/stati/gastrit-ili-gastropatiya-lektsiya/)
Гастрит и гастропатия - различимые либо морфологически (то есть, если проведена биопсия слизистой желудка), либо если пациенту проведена эндоскопия на аппарате с высоким разрешением, дополнительными улучашющими визуализацию настройками и знающим врачом - эндоскопистом, что немаловажно.
Гастрит будет характеризоваться спектром состояний с морфологически подтвержденным воспалением слизистой оболочки желудка , то есть гистологи опишут наличие нейтрофильных лейкоцитов. Остальные же клетки, типа: мононуклеарные клетки (например, лимфоциты, гистиоциты, плазматические клетки), небольшое количество эозинофилов - все они присутствуют в нормальной слизистой, являются как бы сторожами иммунной системы желудка.
А гастропатии, при которых выявляются нарушения гистоархитектоники слизистой оболочки (например, гистологи могут написать в заключении: фовеолярная гиперплазия, гиперплазия мышечной пластинки слизистой оболочки), при этом воспаления не будет совсем или оно будет минимальным ( примеры: реактивная гастропатия, гастропатия, обусловленная дуоденогастральным рефлюксом, портальная гипертензивная гастропатия, эктазия сосудов антрального отдела желудка).
Функциональная диспепсия (ФД) - симптомокомплекс, состоящий из разновариативных жалоб пациента на тяжесть, дискомфорт, чувство раннего насыщения или ненасыщения вовсе, распирание, боль, жжение в верхней части живота (эпигастрии).
А также важно понимать, что структурные изменения слизистой оболочки желудка не связаны с симптомами диспепсии и их тяжестью, а это значит, что у врача нет достоверных клинических симптомов, позволяющих заподозрить атрофию слизистой оболочки желудка на этапе опроса и осмотра.
ФД относится к функциональным заболеваниям желудочно-кишечного тракта (ЖКТ). «Определяющим» центром по таким заболеваниям является Римский фонд. PMID: 27144617.
Функциональные расстройства желудочно-кишечного тракта (ФРЖКТ) — это нарушения взаимодействия между мозгом и кишечником.
Эта группа заболеваний в значительной степени определяется симптомами, не имеющими явной структурной причины.
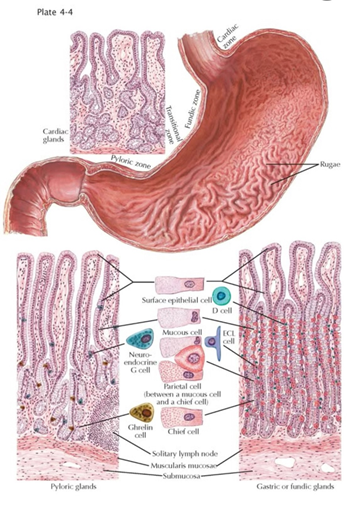
Считается, что в основе ФРЖКТ лежат сложные взаимодействия между различными факторами (микробиом кишечника, нарушения иммунитета слизистой оболочки, висцеральная гиперчувствительность и восприятие боли, нарушение регуляции афферентных сигналов желудочно-кишечного тракта и двигательной функции центральной нервной системы, моторика и чувствительность желудка и двенадцатиперстной кишки). На рис. 2, в его нижней части, где изображены срезы слоев желудка, в подслизистом слое (submucosa), и ниже расположенном мышечном слое и находятся нервные сплетения, сигнализирующие в мозг какими-либо ощущениями. А вышерасположенный слой – и есть слизистая оболочка, изменения структура которой мы можем наблюдать при гастропатии или гастрите.
Что именно происходит у конкретного пациента, требуется ли гастроскопия, какая именно, на каком оборудовании, как часто проводить гастроскопию, нужны ли какие-то дополнительные тесты, в том числе тестирование на хеликобактер пилори-все это определяет врач.
Не занимайтесь самодиагностикой и самолечением!

